Menopauza se danas promatra kao biološki prijelaz s dugoročnim zdravstvenim implikacijama, čime se klinički fokus pomiče s isključivo simptomatskog pristupa prema holističkom i prema prevenciji. Nove smjernice upućuju na individualizaciju terapije, utemeljenost na dokazima i zajedničko donošenje odluka. Vazomotorni simptomi prepoznaju se kao ključni dijagnostički i terapijski kriterij, a ostali simptomi zahtijevaju diferencijalnu dijagnostiku i širu procjenu. Autorica članka: Ana Močić, mag.pharm., univ.spec. kliničke farmacije; inPharma 102, ožujak/travanj 2025.
Menopauza kao biološki prijelaz – nova perspektiva
Menopauza se danas više ne promatra kao jednokratan događaj nego kao dinamičan, individualno varijabilan biološki prijelaz koji obuhvaća perimenopauzu, menopauzu i postmenopauzu. Klinički tijek tranzicije među ženama značajno varira u dobi početka, intenzitetu i trajanju simptoma.
Suvremeni podaci potvrđuju da su vazomotorni simptomi (VMS) – valunzi i noćno znojenje – najpouzdaniji klinički pokazatelji perimenopauze, osobito kod žena s nepravilnim ciklusima ili amenorejom. U velikim populacijskim analizama upravo su vazomotorni simptomi pokazali najveću diskriminacijsku vrijednost u prepoznavanju početka menopauzalne tranzicije, čime se naglasak pomiče s laboratorijskih parametara na kliničku procjenu simptoma.
Ostali simptomi – loše raspoloženje, poremećaji spavanja, muskuloskeletna bol, smanjen libido – česti su, ali nisu specifični za menopauzu i često imaju multifaktorijalnu etiologiju uključujući psihosocijalne, metaboličke i kronične komorbiditete. Upravo je ta nespecifičnost razlog zašto je individualizirana procjena ključna.
Menopauza je, dakle, univerzalno iskustvo s izrazito individualnim tijekom. Kod nekih žena prolazi s minimalnim tegobama, dok kod drugih značajno narušava kvalitetu života i dugoročno zdravlje. Razumijevanje bioloških mehanizama i psihosocijalnih dimenzija ključno je za pružanje skrbi koja je istodobno znanstveno utemeljena i usmjerena na stvarne potrebe žene.
Kako danas definiramo menopauzu?
Menopauza se definira kao trajni prestanak menstruacije, potvrđen nakon dvanaest uzastopnih mjeseci amenoreje, a posljedica je gubitka ovarijske folikularne aktivnosti i smanjenja produkcije estrogena. Iako je riječ o fiziološkom prijelazu u životnom ciklusu žene, menopauza predstavlja duboku biološku i psihosocijalnu prekretnicu. Prosječna dob prirodne menopauze započinje oko 50.-51. godine, no varira ovisno o genetskim, etničkim i okolišnim čimbenicima. Kada nastupi između 40.-44. godine govori se o ranoj menopauzi, dok se menopauza prije 40. godine definira kao prijevremena ovarijska insuficijencija koja može biti spontana ili posljedica kirurškog zahvata, kemoterapije ili drugih medicinskih intervencija. Upravo dob ulaska u menopauzu ima značajne implikacije na dugoročno zdravlje žene.
Klinička slika
Klinička slika menopauze izrazito je heterogena. Najspecifičniji i najčešći simptomi su vazomotorni simptomi – valunzi i noćno znojenje – koji pogađaju više od polovice žena. Oni nastaju zbog promjena u centralnoj termoregulaciji uslijed pada estrogena i mogu trajati godinama, često znatno dulje nego što se ranije smatralo. Intenzitet i učestalost variraju, ali kod mnogih žena dovode do značajnog narušavanja svakodnevnog funkcioniranja.
Poremećaj sna jedan je od najčešćih sekundarnih učinaka vazomotornih simptoma, a ponavljano noćno buđenje zbog znojenja uzrokuje kronični umor, razdražljivost i smanjenu koncentraciju. Uz vazomotorne promjene, velik dio žena razvija genitourinarne simptome koji se danas objedinjeno nazivaju genitourinarni sindrom menopauze. Smanjena estrogenska stimulacija dovodi do stanjivanja vaginalne sluznice, smanjene lubrikacije i povećane osjetljivosti, što rezultira vaginalnom suhoćom i bolnim spolnim odnosom. Česti su i simptomi poput učestalog mokrenja, urgencije ili ponavljanih infekcija mokraćnog sustava, a za razliku od valunga, ako se ne liječe, ti simptomi imaju progresivan tijek i mogu potrajati neograničeno.
Menopauza i mentalno zdravlje
Menopauza je također povezana s promjenama raspoloženja, tjeskobom, osjećajem smanjene mentalne jasnoće i subjektivnim kognitivnim poteškoćama. Iako takvi simptomi nisu specifični isključivo za menopauzu, hormonalne fluktuacije tijekom tranzicije mogu pridonijeti njihovoj izraženosti. Muskulaturu i zglobove zahvaćaju bolovi i ukočenost, a promjene u sastavu tijela, osobito redistribucija masnog tkiva prema abdominalnoj regiji, utječu na samopercepciju i metaboličko zdravlje. Povećanje visceralne adipoznosti povezano je s porastom inzulinske rezistencije i nepovoljnim promjenama lipidnog profila, čime menopauza postaje važna točka u razvoju kardiometaboličkog rizika.
Menopauza i kvaliteta života
Utjecaj menopauze na kvalitetu života može biti dubok. Simptomi ne djeluju samo na fizičko zdravlje, već zahvaćaju emocionalnu stabilnost, seksualno funkcioniranje i profesionalnu produktivnost. Neke žene navode smanjenje radne učinkovitosti zbog umora i poremećaja sna, dok druge ističu poteškoće u intimnim odnosima zbog genitalnih simptoma. Istodobno, percepcija menopauze snažno je oblikovana kulturološkim i društvenim kontekstom. U nekim sredinama ona se doživljava kao prirodna tranzicija, dok je u drugima povezana s osjećajem gubitka mladosti ili ženstvenosti. Socioekonomski status, pristup zdravstvenoj skrbi i stupanj edukacije također utječu na način na koji žena doživljava simptome i nosi se s njima.
Posljedice za cjelokupniorganizam?
Dugoročne zdravstvene implikacije menopauze nadilaze simptomatsku razinu. Pad estrogena povezan je s ubrzanim gubitkom koštane mase i povećanim rizikom osteoporoze i prijeloma, kao i s porastom kardiovaskularnog (KV) rizika. Te posljedice izraženije su kod žena s ranom ili prijevremenom menopauzom, kod kojih dulje razdoblje estrogenskog deficita nosi veći kumulativni učinak na skelet i krvožilni sustav. Stoga menopauza nije samo završetak reproduktivne funkcije, nego i važan biološki marker sistemskog starenja.
Biološke posljedice estrogenskog pada
Pad estrogenske aktivnosti tijekom menopauzalne tranzicije složen je biološki događaj s izraženim multisistemskim posljedicama. Estrogen nije samo reproduktivni hormon, već regulator brojnih fizioloških procesa koji uključuju vaskularnu funkciju, metabolizam lipida i glukoze, održavanje koštane mase te modulaciju neurobioloških mehanizama, osobito onih uključenih u termoregulaciju. Gubitak njegove protektivne uloge stoga pokreće kaskadu promjena koje nadilaze simptomatsku razinu i imaju dugoročne implikacije na zdravlje žene. Suvremeni radovi naglašavaju da menopauza nije izolirani reproduktivni događaj, nego sustavni biološki prijelaz koji utječe na kardiometaboličku, skeletnu i neuroendokrinu ravnotežu organizma.
Jedan od najprepoznatljivijih i najkarakterističnijih kliničkih izraza estrogenskog pada su vazomotorni simptomi. Deregulacija hipotalamičkog termoregulacijskog centra danas se smatra ključnim patofiziološkim mehanizmom njihova nastanka. Estrogen modulira aktivnost neurona u hipotalamusu, koji sudjeluju u održavanju temperaturne homeostaze, a njegov pad dovodi do suženja termoneutralne zone i povećane osjetljivosti na minimalne promjene tjelesne temperature. U tom procesu posebnu ulogu ima neurokinin B signalni sustav koji djeluje putem NK3 receptora u KNDy neuronima. Pojačana aktivnost tog sustava u estrogenskom deficitu povezana je s nastankom valunga i noćnog znojenja, a upravo je razumijevanje tog mehanizma omogućilo razvoj novih ciljano usmjerenih terapija. Time su vazomotorni simptomi dobili i neurobiološko objašnjenje koje ih jasno povezuje s centralnom regulacijom.
Osim termoregulacijskih promjena, estrogenski pad povezan je s ubrzanim gubitkom koštane mase, što se pripisuje pojačanoj aktivnosti osteoklasta i smanjenoj koštanoj formaciji. U prvih nekoliko godina nakon menopauze dolazi do naglog pada mineralne gustoće kosti, čime se povećava rizik osteoporoze i prijeloma. Paralelno se bilježi porast kardiometaboličkog rizika, uključujući nepovoljne promjene lipidnog profila, porast inzulinske rezistencije i redistribucija masnog tkiva prema visceralnoj adipoznosti. Ta centralna akumulacija masnog tkiva dodatno pojačava upalne i metaboličke procese, čime menopauza postaje prekretnica u KV riziku. Navedene promjene nisu prolazne ni isključivo simptomatske, već imaju dugoročne implikacije na morbiditet i mortalitet, osobito u kontekstu KV bolesti i osteoporotičnih prijeloma.
Vazomotorni simptomi kao klinički kriterij
Danas su vazomotorni simptomi prepoznati kao najpouzdaniji klinički indikator menopauzalne tranzicije. Podaci iz recentnih kohortnih istraživanja pokazuju da su valunzi i noćno znojenje često dugotrajniji nego što se ranije smatralo te da mogu potrajati više godina nakon završetka menstruacije. Njihova prisutnost snažno je povezana s poremećajem sna, promjenama raspoloženja i smanjenjem kvalitete života, čime prelaze granice “neugodnog simptoma” i postaju važan klinički kriterij za terapijsku intervenciju. Upravo njihovo pravodobno prepoznavanje omogućuje ranu i ciljanu terapiju.

Menopauzalna hormonska terapija (MHT)
MHT i dalje ostaje najučinkovitiji oblik liječenja vazomotornih simptoma i urogenitalne atrofije. Osim simptomatskog učinka ima i dodatne koristi, uključujući smanjenje gubitka koštane mase i prevenciju osteoporoze. Postoje i podaci koji upućuju na potencijalno povoljan učinak na kardiometaboličke parametre, osobito kada se terapija započne na vrijeme, odnosno u ranoj postmenopauzi, prije nego što se razviju značajne aterosklerotske promjene. Međutim, u većini zemalja MHT je formalno odobrena za žene u postmenopauzi, dok su jasne i standardizirane smjernice za perimenopauzu još uvijek nedostatne. To upućuje na potrebu za daljnjim istraživanjima i preciznijim kliničkim algoritmima.
Suvremeni pristup hormonskoj terapiji temelji se na individualizaciji. Procjenjuju se dob pacijentice, vrijeme proteklo od menopauze, KV i onkološki rizik te osobne vrijednosti i preferencije žene. Koncept zajedničkog donošenja odluka postao je središnji element kliničke prakse, naglašavajući važnost informiranog dijaloga između liječnika i pacijentice.
Nove nehormonske terapije: antagonisti neurokinin B receptora
Razvoj antagonista neurokinin-3 receptora predstavlja značajan napredak u nehormonskom liječenju vazomotornih simptoma. Ti lijekovi djeluju centralno, modulirajući hipotalamičke mehanizme termoregulacije bez estrogenskog učinka na periferna tkiva. Posebno su važni za žene s kontraindikacijama za estrogensku terapiju, uključujući one s povećanim rizikom od karcinoma dojke ili s anamnezom hormonski ovisnih malignih tumora. Iako su klinički rezultati obećavajući, dugoročni sigurnosni podaci i izravne usporedbe s MHT još su u razvoju. Ti lijekovi dostupni su u EU, ali još uvijek nemaju rutinsku kliničku primjenu u Hrvatskoj. Postupno uvođenje očekuje se u razdoblju od 1-3 godine.
Rana menopauza i prijevremena ovarijska insuficijencija
Posebnu kliničku skupinu čine žene s ranom menopauzom i prijevremenom ovarijskom insuficijencijom kod kojih je estrogenski deficit izraženiji i dugotrajniji, što rezultira povećanim rizikom od osteoporoze, KV bolesti i metaboličkih poremećaja u mlađoj životnoj dobi. U toj populaciji hormonska nadomjesna terapija često ima protektivnu ulogu i preporučuje se do prosječne dobi prirodne menopauze, uz individualnu procjenu rizika. U takvim slučajevima terapija nije samo simptomatska, nego i preventivna.
Dob menopauze i dugovječnost
Dob ulaska u menopauzu povezana je s genetskim, etničkim i životnim čimbenicima. Kasnija menopauza povezana je s boljim općim zdravstvenim ishodima i većom dugovječnošću, što potvrđuje da menopauza odražava širi biološki proces starenja. Ona se danas promatra kao marker sistemskog biološkog starenja, a ne samo kao završetak reproduktivne funkcije.
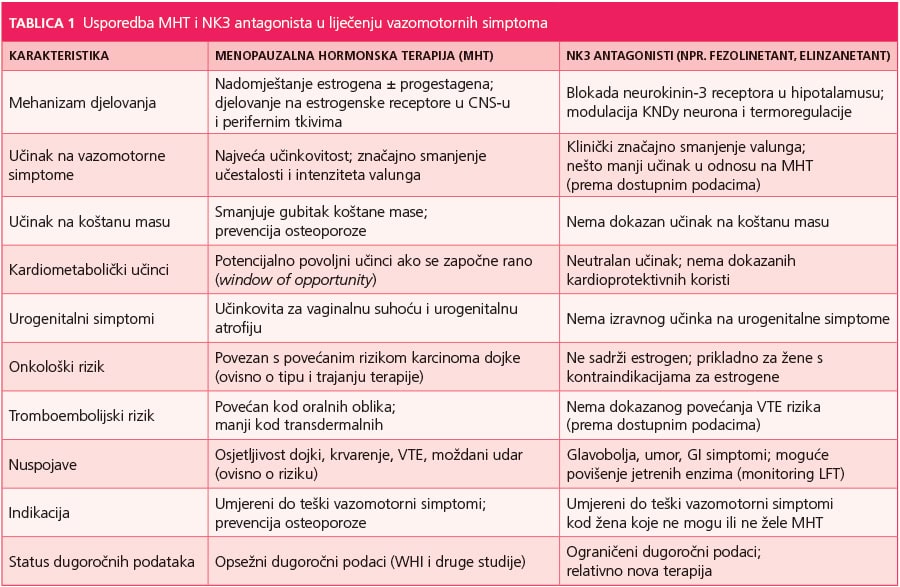
MHT vs neurokinin antagonisti (NK3)
MHT i neurokinin antagonisti (najviše podataka imamo za NK3 antagoniste poput fezolinetanta) dva su konceptualno različita pristupa liječenju vazomotornih simptoma. MHT djeluje “uzročno” u smislu nadoknade estrogenskog deficita, čime utječe na više organskih sustava, dok NK3 antagonisti ciljaju specifičan neuroendokrini mehanizam termoregulacije u hipotalamusu (KNDy neuroni / neurokinin B signalizacija) i time selektivno smanjuju valunge i noćno znojenje bez hormonskog učinka.
Učinkovitost na vazomotorne simptome: MHT ostaje najdjelotvornija terapija za umjerene do teške vazomotorne simptome i u većini smjernica se navodi kao zlatni standard, osobito za žene koje su unutar približno 10 godina od menopauze i bez kontraindikacija. NK3 antagonisti poput fezolinetanta u randomiziranim studijama također pokazuju značajno smanjenje učestalosti i težine valunga s relativno brzim početkom učinka, a učinak je konzistentno bolji od placeba. Klinički, NK3 antagonisti posebno su vrijedni kada je cilj kontrolirati valunge, bez potrebe (ili bez mogućnosti) za hormonskim djelovanjem.
Što sve “pokriva” terapija: MHT ne djeluje samo na valunge, nego je najučinkovitija i za urogenitalne simptome (vaginalna suhoća, urogenitalna atrofija) te smanjuje gubitak koštane mase i rizik osteoporotičnih prijeloma tijekom primjene. Nasuprot tome, NK3 antagonisti su primarno razvijeni za vazomotorne simptome, ne smatraju se terapijom za urogenitalnu atrofiju niti za zaštitu kostiju. U praksi to znači da će dio žena na NK3 antagonistu i dalje trebati dodatno ciljano liječenje urogenitalnih simptoma (npr. lokalna terapija) i liječenje koštanog rizika.
Sigurnost i kontraindikacije – ključna razlika u profilu rizika: MHT nosi specifične rizike i kontraindikacije povezane s hormonskom izloženošću (npr. tromboembolijski rizik, određene hormonski ovisne malignosti, specifične KV situacije ovisno o dobi i vremenu od menopauze). Zbog toga je kod MHT nužna individualna procjena i tzv. shared decision-making. NK3 antagonisti su bez hormona i zato su osobito relevantni za žene koje ne smiju ili ne žele MHT (npr. žene s visokim rizikom za karcinom dojke ili s kontraindikacijama za estrogensku terapiju). Međutim, NK3 antagonisti imaju vlastiti sigurnosni “potpis” – za fezolinetant je važan aspekt praćenje jetrenih enzima, jer su zabilježene rijetke, ali klinički važne jetrene nuspojave te se u praksi naglašava potreba za nadzorom prema uputama lijeka.
Kako praktično birati terapiju: Ako žena ima umjerene do teške valunge i istodobno ima vaginalne simptome ili povišen rizik gubitka koštane mase, a nema kontraindikacija, MHT često daje “širi” terapijski benefit, jer rješava više aspekata menopauze odjednom. Ako je primarni problem vazomotorna simptomatologija, a MHT je kontraindicirana ili neželjena, NK3 antagonisti nude suvremenu, ciljanu i učinkovitu nehormonsku opciju.
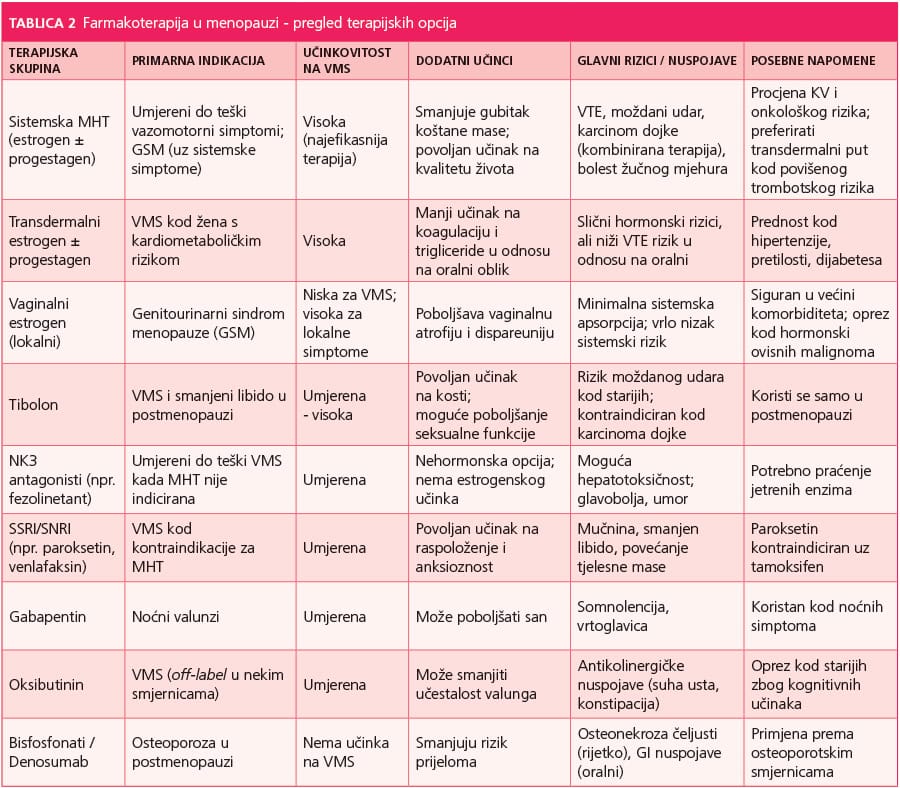
Nuspojave terapije u menopauzi: suvremeni dokazi i kliničke implikacije
Liječenje simptoma menopauze značajno je napredovalo posljednjih desetljeća, ali se istodobno razvila sofisticiranija svijest o rizicima terapije. Menopauzalna hormonska terapija (MHT) i nove nehormonske opcije, osobito antagonisti neurokinin B receptora, imaju različite sigurnosne profile koji zahtijevaju pažljivu procjenu koristi i rizika. Najnoviji sustavni pregledi, smjernice i regulatorne preporuke naglašavaju potrebu za individualiziranom procjenom i redovitim praćenjem sigurnosti.
Menopauzalna hormonska terapija – rizici
Venska tromboembolija i moždani udar – Najčešći rizik povezan s oralnom estrogenskom terapijom je povećan rizik od venske tromboembolije (VTE) i ishemijskog moždanog udara. Podaci iz Women’s Health Initiative (WHI) te recentne Cochrane analize potvrđuju da oralni estrogen, sa ili bez progestina, povećava rizik tromboembolijskih događaja, osobito kod starijih žena i onih koje započinju terapiju više godina nakon menopauze. Važno je istaknuti da je rizik izraženiji kod oralnih formulacija, a niži kod transdermalnih pripravaka (zbog izbjegavanja first-pass jetrenog učinka) te potencijalno niži kod nižih doza. Međutim, dugoročni sigurnosni podaci za niže doze i transdermalne oblike još su ograničeni.
Rizik od karcinoma dojke – Kombinirana estrogen-progestinska terapija povezana je s povećanim rizikom karcinoma dojke, dok estrogenska monoterapija (kod žena bez maternice) pokazuje drugačiji profil rizika. Rizik je ovisan o trajanju primjene, a veći je kod dulje upotrebe. Također, pokazalo se da je reverzibilan nakon prestanka terapije (uz postupno smanjenje rizika). Taj aspekt posebno je važan kod žena s osobnom ili obiteljskom anamnezom hormonski ovisnih malignoma.
Bolesti žučnog mjehura – I estrogenska monoterapija i kombinirana terapija povećavaju rizik kolelitijaze, kolecistitisa kao i potrebe za kolecistektomijom. Taj rizik povezan je s estrogenskim učinkom na metabolizam kolesterola i sastav žuči.
Urinarna inkontinencija – Paradoksalno, MHT može povećati incidenciju urinarne inkontinencije, osobito stresne inkontinencije, što je aspekt koji se često zanemaruje u kliničkoj komunikaciji.
Ograničenje primjene u primarnoj prevenciji
Prema USPSTF smjernicama, MHT se ne preporučuje za primarnu prevenciju kroničnih bolesti (kardiovaskularnih, demencije itd.) zbog nepovoljnog omjera koristi i rizika u toj indikaciji. Naglasak je danas isključivo na simptomatskoj terapiji.
Neurokinin B antagonisti: novi sigurnosni izazovi
Razvoj antagonista NK3 receptora predstavlja jedan od najvećih napredaka u nehormonskom liječenju vazomotornih simptoma. Međutim, s njihovom primjenom pojavili su se novi sigurnosni aspekti.
Hepatotoksičnost – nova i ključna zabrinutost – Fezolinetant je povezan s umjerenim povišenjem jetrenih enzima kao i rijetkim, ali potencijalno ozbiljnim oštećenjem jetre, zbog čega je FDA propisala obavezno mjerenje jetrenih enzima prije početka terapije kao i periodično praćenje tijekom liječenja. Iako je incidencija teške hepatotoksičnosti niska, regulatorne mjere odražavaju potrebu za oprezom u širokoj populaciji.
Elinzanetant – potencijalno povoljniji profil? – Taj dualni NK1/NK3 antagonist, u fazi IIb studija nije pokazao signal hepatotoksičnosti povezan s lijekom, međutim dugoročni sigurnosni podaci još nisu dostupni, a potrebna su i real-world iskustva. Zato je prerano govoriti o definitivno povoljnijem sigurnosnom profilu.
Ostale nuspojave NK antagonista – Najčešće prijavljene nuspojave su glavobolja, umor, blagi gastrointestinalni simptomi. One su uglavnom blage i prolazne, ali nadzor ostaje ključan.
Ostale nehormonske opcije
SSRI/SNRI – Često korišteni kod žena s kontraindikacijama za MHT. Moguće nuspojave su smanjeni libido, povećanje tjelesne mase, mučnina, emocionalna “otupjelost”.
Na koje komorbiditete moramo paziti pri upotrebi hormonski nadomjesne terapije?
MHT ostaje najučinkovitiji oblik liječenja vazomotornih simptoma i urogenitalne atrofije, no njezina primjena zahtijeva jasno definirane granice sigurnosti, osobito kod žena s određenim komorbiditetima. Suvremene smjernice, uključujući preporuke Američkog društva opstetričara i ginekologa (ACOG), recentne JAMA i JACC analize te pregled Women’s Health Initiative studija, dosljedno naglašavaju da postoje kliničke situacije u kojima je MHT kontraindicirana zbog nepovoljnog omjera koristi i rizika. Te kontraindikacije proizlaze iz biologije estrogenskog djelovanja, epidemioloških podataka i randomiziranih kliničkih ispitivanja.
Jedna od najvažnijih apsolutnih kontraindikacija odnosi se na hormonski ovisne maligne bolesti, osobito karcinom dojke i na estrogen osjetljiv karcinom endometrija. Estrogen ima proliferativni učinak na tkiva koja eksprimiraju estrogenske receptore, uključujući dojku i endometrij, te može poticati rast preostalih malignih ili premalignih stanica. Kod žena s anamnezom hormonski ovisnog karcinoma, dodatna hormonska stimulacija može povećati rizik recidiva, zbog čega se MHT u pravilu izbjegava u toj populaciji. Slično tome, neobjašnjeno vaginalno krvarenje predstavlja klinički alarm koji zahtijeva dijagnostičku obradu prije razmatranja bilo kakve hormonske terapije, jer može biti prvi znak endometrijske patologije.
KV bolesti također su ključan sigurnosni aspekt. Žene s prethodnim aterosklerotskim KV događajima poput infarkta miokarda ili moždanog udara, smatraju se rizičnom skupinom kojoj je MHT kontraindicirana. Randomizirani podaci i dugoročna praćenja pokazali su da estrogenska terapija, osobito oralna, može povećati rizik venske tromboembolije i ishemijskog moždanog udara, osobito u starijoj dobi ili kod žena koje započinju terapiju znatno nakon menopauze. Kod žena s već postojećom aterosklerozom ili visokim kardiometaboličkim rizikom dodatna hormonska modulacija može destabilizirati vaskularni sustav, što opravdava oprez ili izbjegavanje terapije. Posebno su rizične žene s anamnezom venske tromboembolije ili plućne embolije, kao i one s visokorizičnim nasljednim ili stečenim trombofilijama poput deficita antitrombina, proteina C ili proteina S. U tim je slučajevima estrogenska terapija povezana s neprihvatljivo povišenim trombotskim rizikom.
Teška aktivna bolest jetre također je kontraindikacija za MHT. Budući da se estrogeni metaboliziraju u jetri i utječu na sintezu brojnih proteina plazme, njihova primjena može dodatno opteretiti kompromitiranu jetrenu funkciju. Osim toga, promjene u sintezi koagulacijskih faktora i lipoproteina mogu dodatno destabilizirati metaboličku ravnotežu kod žena s hepatopatijama. Stoga je prije započinjanja terapije nužna procjena jetrene funkcije, osobito kod žena s anamnezom hepatitisa, ciroze ili drugih kroničnih jetrenih bolesti.
Važno je istaknuti da MHT nije indicirana za primarnu ili sekundarnu prevenciju kroničnih bolesti, uključujući KV bolesti i osteoporozu, bez prisutnih simptoma menopauze. Preporuke USPSTF-a i analiza Women’s Health Initiative jasno su pokazale da potencijalne koristi u smislu smanjenja prijeloma ili određenih metaboličkih učinaka ne nadmašuju rizike kada se terapija koristi isključivo u preventivne svrhe. Time je suvremeni pristup jasno usmjeren na simptomatsko liječenje, a ne na dugoročnu profilaktičku primjenu hormona.
Kod žena s komorbiditetima poput pretilosti, hipertenzije ili šećerne bolesti, terapijska odluka zahtijeva individualiziranu procjenu rizika. U takvim situacijama transdermalni estrogen često se preferira u odnosu na oralne oblike zbog nižeg utjecaja na jetru i potencijalno manjeg trombotskog rizika, iako se ni transdermalni pripravci ne smatraju potpuno bez rizika.
Posebnu skupinu čine žene s prijevremenom ili ranom menopauzom, kod kojih MHT može imati zaštitnu ulogu do prosječne dobi prirodne menopauze, pod uvjetom da ne postoje kontraindikacije poput hormonski ovisnih malignih tumora ili tromboembolijske bolesti. U toj populaciji koristi hormonske nadomjesne terapije često nadmašuju rizike, jer rana estrogenska deprivacija nosi povećani rizik osteoporoze i KV komplikacija.
U konačnici, suvremene smjernice naglašavaju da je MHT kontraindicirana kod žena s hormonski osjetljivim karcinomima, neobjašnjenim vaginalnim krvarenjem, prethodnim aterosklerotskim KV događajima, moždanim udarom ili TIA-om, venskom tromboembolijom, teškom aktivnom jetrenom bolešću i visokorizičnim trombofilijama. Istodobno, kod žena bez tih kontraindikacija terapija može biti sigurna i učinkovita uz pažljivu selekciju doze, načina primjene i trajanja liječenja. Središnje mjesto u kliničkoj odluci zauzima informirani razgovor s pacijenticom u kojem se jasno komuniciraju potencijalne koristi i rizici, te se odluka donosi zajednički, uz plan praćenja i redovitu reevaluaciju terapije.
MHT i interakcije
Menopauzalna hormonska terapija (MHT) u kliničkoj praksi sve češće se propisuje ženama koje istodobno imaju kardiometaboličke, neurološke ili druge kronične bolesti te uzimaju više lijekova. Upravo zato pitanje interakcija postaje jednako važno kao i pitanje same indikacije. Najveći dio klinički relevantnih interakcija odnosi se na oralne estrogenske pripravke koji prolaze kroz jetru i podliježu metabolizmu putem citokromskog sustava, osobito CYP3A4 izoenzima. Taj mehanizam objašnjava zašto su oralni oblici MHT najosjetljiviji na farmakokinetičke promjene uzrokovane drugim lijekovima.
Oralni estrogen nakon apsorpcije iz gastrointestinalnog trakta ulazi u portalnu cirkulaciju i izravno dolazi u jetru gdje se metabolizira putem CYP3A4. Ako pacijentica istodobno uzima snažne induktore CYP3A4 poput karbamazepina, fenitoina, rifampicina ili pripravaka gospine trave, dolazi do ubrzanog metabolizma estrogena. Posljedica toga može biti smanjenje serumskih koncentracija hormona i gubitak terapijskog učinka – primjerice slabija kontrola vazomotornih simptoma ili nestabilno krvarenje kod kombiniranih režima. Klinički, to se može manifestirati “iznenadnim povratkom” valunga ili nepravilnim krvarenjem, što ponekad dovodi do nepotrebnog povećanja doze, iako je pravi uzrok interakcija.
Suprotna situacija nastaje kod primjene snažnih inhibitora CYP3A4 poput ketokonazola, itrakonazola ili pojedinih makrolidnih antibiotika. U tom slučaju metabolizam estrogena je usporen, koncentracije u plazmi rastu i povećava se rizik nuspojava – uključujući osjetljivost dojki, mučninu, zadržavanje tekućine, ali i ozbiljnije komplikacije poput tromboembolijskih događaja kod predisponiranih žena. Takve interakcije osobito su relevantne kod žena koje uzimaju antimikotike ili antibiotike u duljim terapijskim ciklusima te kod onih s već postojećim KV rizičnim čimbenicima.
Posebno osjetljivo područje odnosi se na interakciju estrogena s antikoagulantnom terapijom. Budući da estrogeni povećavaju sklonost trombozi modulacijom koagulacijskih faktora i fibrinolize, njihova primjena kod žena koje već uzimaju varfarin ili direktne oralne antikoagulanse (DOAC) zahtijeva dodatni oprez. Interakcija nije uvijek predvidiva. U nekim slučajevima može doći do promjena u farmakodinamičkoj ravnoteži – estrogen potencira protrombotski učinak, dok antikoagulans pokušava održati antitrombotsku zaštitu. U terapiji varfarinom mogu se javiti oscilacije u INR-u, osobito pri uvođenju ili prekidu MHT, što zahtijeva češće laboratorijsko praćenje. Kod DOAC terapije laboratorijsko praćenje nije rutinsko, pa je klinički nadzor simptoma krvarenja ili tromboze ključan. Kod žena s anamnezom tromboembolije već je sama indikacija za MHT često upitna, a u situacijama kada se razmatra transdermalni oblik i pažljivo praćenje, nužno je multidisciplinarno odlučivanje.
Interakcije s antihipertenzivima također imaju kliničku težinu. Estrogen može dovesti do blagog porasta krvnog tlaka putem nekoliko mehanizama: zadržavanja natrija i tekućine, utjecaja na renin-angiotenzin-aldosteronski sustav te modulacije vaskularnog tonusa. Kod žena s već postojećom hipertenzijom to može značiti potrebu za prilagodbom antihipertenzivne terapije ili učestalije praćenje tlaka nakon uvođenja MHT. Iako taj učinak nije univerzalan niti izražen kod svih žena, njegova klinička važnost raste u populaciji s višestrukim kardiometaboličkim rizičnim čimbenicima.
Prednost transdermalnih i vaginalnih estrogenskih pripravaka
Upravo zbog tih farmakokinetičkih i farmakodinamičkih interakcija, transdermalni oblici estrogena predstavljaju važnu alternativu. Budući da zaobilaze jetreni first-pass metabolizam, njihova ovisnost o CYP3A4 sustavu znatno je manja. Time se smanjuje potencijal za interakcije s induktorima i inhibitorima jetrenih enzima, a istodobno je manji učinak na sintezu koagulacijskih faktora. To ih čini prikladnijim izborom za žene na politerapiji, osobito one koje uzimaju antiepileptike, antituberkulotike, antifungalne lijekove ili druge snažne modifikatore jetrenog metabolizma. Iako transdermalni estrogen nije potpuno lišen sistemskih učinaka, njegov stabilniji farmakokinetički profil pridonosi predvidljivijem sigurnosnom okviru.
Vaginalni estrogenski pripravci su zaseban slučaj. Zbog minimalne sistemske apsorpcije, oni u pravilu ne postižu značajne koncentracije u plazmi te se smatraju sigurnima u većini situacija politerapije. Interakcije putem CYP sustava gotovo su zanemarive, a učinak na koagulaciju ili krvni tlak minimalan. Upravo zato se lokalna terapija često preporučuje ženama s kontraindikacijama za sistemsku MHT, osobito kada su dominantni urogenitalni simptomi.
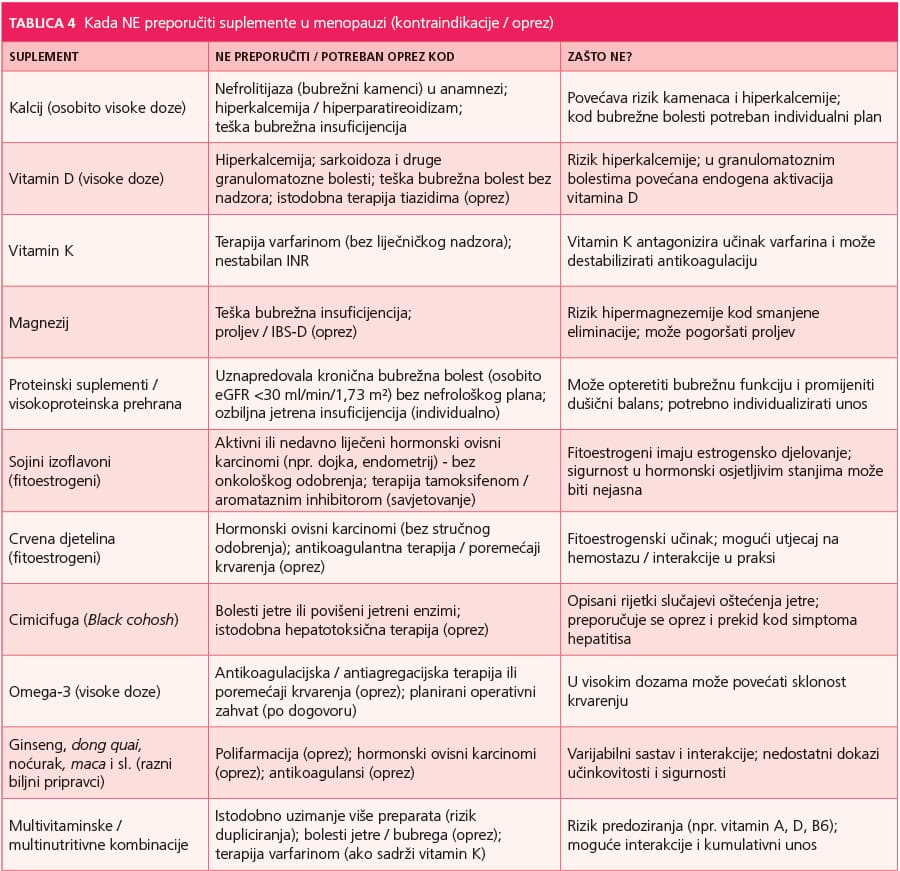
Znanost o suplementaciji u menopauzi
Primjena dodataka prehrani u perimenopauzi i postmenopauzi često se percipira kao “sigurna” i prirodna alternativa hormonskoj terapiji, no njihova uloga u očuvanju zdravlja znatno je složenija i zahtijeva individualizirani pristup. Učinkovitost i sigurnost tih pripravaka ovise o vrsti suplementa, početnom nutritivnom statusu žene, prisutnosti komorbiditeta te konkretnim zdravstvenim ciljevima – bilo da je riječ o prevenciji osteoporoze, ublažavanju vazomotornih simptoma ili općem osjećaju vitalnosti.
Jedno od najčešćih područja primjene dodataka prehrani u menopauzi odnosi se na očuvanje koštanog zdravlja. Pad estrogenske aktivnosti ubrzava koštanu resorpciju i povećava rizik osteoporoze, što opravdava interes za suplementaciju kalcijem, vitaminima D i K, magnezijem i proteinima. Ipak, podaci iz velikih randomiziranih studija, uključujući Women’s Health Initiative, pokazuju da rutinska suplementacija kalcijem i vitaminom D u svrhu prevencije prijeloma nije univerzalno indicirana za sve žene u postmenopauzi. Korist se primarno očekuje kod žena koje ne postižu preporučene dnevne unose putem prehrane. Drugim riječima, suplementacija ima smisla kada postoji nutritivni deficit, a ne kao opća populacijska strategija bez procjene unosa i rizika.
Nedavne mrežne meta-analize sugeriraju da suplementi poput vitamina D i K, kalcija i proteina mogu povoljno djelovati na biljege koštanog metabolizma, odnosno smanjiti markere koštane resorpcije i potaknuti koštanu formaciju. Međutim, prijenos tih biokemijskih učinaka na klinički ishod – smanjenje prijeloma – ostaje manje jasan. Učinak može varirati ovisno o dobi, početnoj gustoći kosti, komorbiditetima i razini tjelesne aktivnosti. Stoga suplementacija može biti dio šire strategije očuvanja koštane mase, ali ne zamjenjuje dokazano učinkovite terapije kod žena s dijagnosticiranom osteoporozom.
Drugo važno područje interesa odnosi se na ublažavanje simptoma menopauze biljnim pripravcima, osobito onima koji sadrže fitoestrogene poput sojinih izoflavona, crvene djeteline ili cimicifuge. Sustavni pregledi i meta-analize pokazuju da ti pripravci mogu imati umjeren učinak na smanjenje vazomotornih simptoma, no kvaliteta dokaza varira, a rezultati su često heterogeni. U pravilu je njihova učinkovitost manja u usporedbi s MHT. Ipak, kod žena s blagim do umjerenim simptomima ili kod onih koje ne žele ili ne smiju koristiti hormonsku terapiju, takvi pripravci, uz odgovarajuće savjetovanje, mogu predstavljati alternative.
Važno je naglasiti da fitoestrogeni, iako “biljnog” podrijetla, djeluju na estrogenske receptore i mogu imati estrogenski ili antiestrogenski učinak ovisno o tkivu i koncentraciji. To otvara pitanje sigurnosti kod žena s hormonski ovisnim malignim bolestima ili visokim onkološkim rizikom. Dok su dostupni podaci ograničeni i često neujednačeni, potreban je oprez pri preporuci takvih pripravaka ženama s anamnezom karcinoma dojke ili endometrija. Nadalje, kvaliteta i standardizacija biljnih dodataka mogu značajno varirati, a tržište dodataka prehrani često nije regulirano jednako strogo kao farmaceutski pripravci.
Multinutritivne kombinacije koje sadrže vitamine B skupine, antioksidanse i druge mikronutrijente ponekad se promoviraju kao sredstva za poboljšanje energije, raspoloženja i općeg zdravlja u menopauzi. Međutim, njihova korist u pravilu proizlazi iz korekcije specifičnih nedostataka, a ne iz univerzalnog anti-age učinka. Pretjerana ili nekontrolirana primjena može dovesti do hipervitaminoza ili interakcija s lijekovima, osobito kod žena koje već uzimaju terapiju za KV, metaboličke ili onkološke bolesti.
U širem kontekstu, suplementacija u menopauzi treba se promatrati kao dio integrativnog pristupa koji uključuje uravnoteženu prehranu, tjelesnu aktivnost, održavanje zdrave tjelesne mase i upravljanje kardiometaboličkim čimbenicima rizika. Dodaci prehrani mogu djelomično nadoknaditi nutritivne praznine i podržati određene aspekte zdravlja, ali ne bi trebali zamijeniti terapije čija je učinkovitost potvrđena u velikim kliničkim ispitivanjima, osobito kada su simptomi izraženi ili kada postoji visok rizik osteoporotičnih prijeloma.
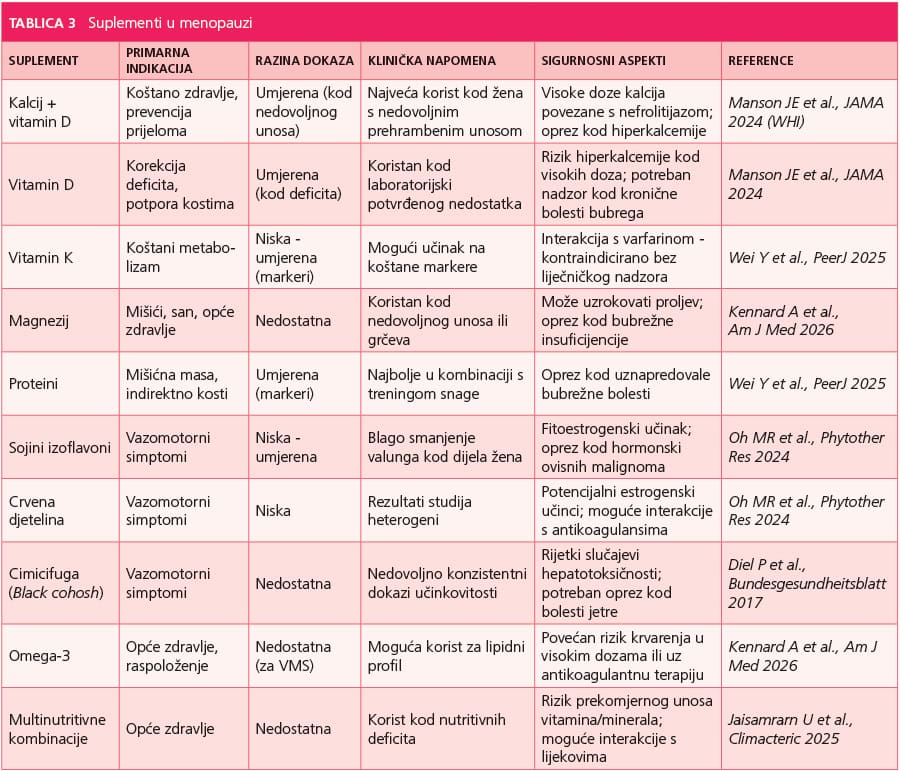
Što možemo zaključiti o suplementaciji?
Zaključno, suplementi u razdoblju perimenopauze i postmenopauze imaju potencijalnu, ali ograničenu i kontekstualnu ulogu. Njihova primjena mora biti individualizirana, uz procjenu nutritivnog statusa, simptoma, komorbiditeta i terapijskih ciljeva. Dok određeni nutrijenti mogu pridonijeti očuvanju koštanog zdravlja, a neki biljni pripravci ublažiti simptome, njihova učinkovitost i sigurnost nisu univerzalne niti usporedive s hormonskom terapijom kada je ona indicirana. Klinička odluka stoga treba biti utemeljena na dokazima, uz otvorenu komunikaciju s pacijenticom o očekivanim koristima, mogućim rizicima i realnim terapijskim ciljevima.
Integrirani pristup očuvanju kvalitete života
Menopauza nije uniformno iskustvo, već heterogeno biopsihosocijalno razdoblje u kojem kvaliteta života ovisi o međudjelovanju intenziteta simptoma, mentalnog zdravlja, životnog stila i sociodemografskih čimbenika. Istodobno, važno je naglasiti da menopauza sama po sebi nije sinonim za smanjenu kvalitetu života. Brojne žene prolaze tranziciju uz blage simptome i zadržavaju stabilno psihofizičko funkcioniranje, osobito kada su prisutni zaštitni čimbenici poput redovite tjelesne aktivnosti i zdrave tjelesne mase. Mentalno zdravlje pritom ima ključnu ulogu, pa tako depresivni i anksiozni simptomi značajno pogoršavaju subjektivnu percepciju kvalitete života, neovisno o jačini somatskih simptoma.
Dokazi upućuju na to da se kvaliteta života kod dijela žena u postmenopauzi može djelomično poboljšati s postupnim slabljenjem vazomotornih tegoba, no perzistentni simptomi, komorbiditeti i nepovoljni životni stilovi mogu dugoročno održavati smanjenu kvalitetu života.
Klinički gledano, menopauza zahtijeva individualizirani, multidimenzionalni pristup. Hormonska terapija, nehormonske farmakološke opcije, ciljana terapija specifičnih simptoma kao i intervencije usmjerene na mentalno zdravlje i životne navike, imaju potencijal značajno poboljšati kvalitetu života žena s opisanim simptomima. Upravo personalizirano upravljanje simptomima, uz kontinuiranu edukaciju i podršku, predstavlja temelj suvremenog pristupa menopauzi. Uz pravodobno prepoznavanje tegoba i odgovarajuće intervencije moguće je očuvati, pa čak i unaprijediti kvalitetu života u tom životnom razdoblju.
Literatura:
- Crandall CJ, Mehta JM, Manson JE. Management of menopausal symptoms: A review. JAMA. 2023;329(5):405-420. doi:10.1001/jama.2022.24140.
- Davis SR, Pinkerton J, Santoro N, Simoncini T. Menopause: Biology, consequences, supportive care, and therapeutic options. Cell. 2023;186(19):4038-4058. doi:10.1016/j.cell.2023.08.016.
- Davis SR, Baber RJ. Treating menopause – MHT and beyond. Nat Rev Endocrinol. 2022;18(8):490-502. doi:10.1038/s41574-022-00685-4.
- Mishra GD, Davies MC, Hillman S, et al. Optimising health after early menopause. Lancet. 2024;403(10430):958-968. doi:10.1016/S0140-6736(23)02800-3.
- Santoro N, Roeca C, Peters BA, Neal-Perry G. The menopause transition: Signs, symptoms, and management options. J Clin Endocrinol Metab. 2021;106(1):1-15. doi:10.1210/clinem/dgaa764.
- Duralde ER, Sobel TH, Manson JE. Management of perimenopausal and menopausal symptoms. BMJ. 2023;382:e072612. doi:10.1136/bmj-2022-072612.
- Lobo RA, Gompel A. Management of menopause: A view towards prevention. Lancet Diabetes Endocrinol. 2022;10(6):457-470. doi:10.1016/S2213-8587(21)00269-2.
- Islam RM, Bond M, Ghalebeigi A, et al. Prevalence and severity of symptoms across the menopause transition. Lancet Diabetes Endocrinol. 2025;13:765-776.
- Hickey M, LaCroix AZ, Doust J, et al. An empowerment model for managing menopause. Lancet. 2024;403:947-957. doi:10.1016/S0140-6736(23)02799-X.
- Pinkerton JV. Hormone therapy for postmenopausal women. N Engl J Med. 2020;382(5):446-455. doi:10.1056/NEJMcp1714787.
- Manson JE, Crandall CJ, Rossouw JE, et al. The Women’s Health Initiative randomized trials and clinical practice: A review. JAMA. 2024;331(20):1748-1760. doi:10.1001/jama.2024.6542.
- Mangione CM, Barry MJ, et al. Hormone therapy for the primary prevention of chronic conditions: USPSTF recommendation statement. JAMA. 2022;328(17):1740-1746. doi:10.1001/jama.2022.18625.
- Shufelt CL, Manson JE. Menopausal hormone therapy and cardiovascular disease. J Clin Endocrinol Metab. 2021;106(5):1245-1254. doi:10.1210/clinem/dgab042.
- Huang AJ, Faubion S, Grady D. Nonhormonal treatment of menopausal vasomotor symptoms. JAMA Intern Med. 2025;185(7):874-875.
- Panay N, Joffe H, Maki PM, et al. Elinzanetant for treatment of vasomotor symptoms associated with menopause. JAMA Intern Med. 2025;185(11):1319-1327. doi:10.1001/jamainternmed.2025.4421.
- Hager M, Goldstein T, Fitz V, Ott J. Neurokinin-1/-3 receptor antagonists for menopausal vasomotor symptoms. Expert Opin Pharmacother. 2024;25(7):783-789. doi:10.1080/14656566.2024.2358131.
- Kennard A, Saunders KT. Integrative approaches to perimenopause. Am J Med. 2026;S0002-9343(26)00013-6. doi:10.1016/j.amjmed.2025.12.024.
- Wei Y, Lei C, Zhong Y, Shen H. Effects of dietary supplements on bone turnover markers after menopause: Network meta-analysis. PeerJ. 2025;13:e19882. doi:10.7717/peerj.19882.
- Oh MR, Park JH, Park SK, Park SH. Plant-derived dietary supplements for menopausal symptoms: Systematic review and meta-analysis. Phytother Res. 2024;38(3):1294-1309. doi:10.1002/ptr.8112.
- Diel P, Kurrat A, Oden C, Hanke L. Risks and benefits of nutritional supplements for postmenopausal complaints. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 2017;60(3):297-304.
- Kapoor E, Kling JM, Lobo AS, Faubion SS. Menopausal hormone therapy in women with medical conditions. Best Pract Res Clin Endocrinol Metab. 2021;35(6):101578. doi:10.1016/j.beem.2021.101578.
- Fasero M, Quereda F, Andraca L, Coronado PJ. Pharmacological interactions and menopausal hormone therapy. Menopause. 2023;30(8):873-880. doi:10.1097/GME.0000000000002219.
